
পর্যায় সারণি মনে রাখার কৌশল | ১০ মিনিটেই শিখে ফেলো পর্যায় সারণি
আপনি কি পর্যায় সারণি মনে রাখার চেস্টা করতিছেন? কিন্তু পর্যায় সারণি মনে রাখতে পারছেন না? চিন্তা করবেন না এই আর্টিকেলটিতে আমি পর্যায় সারণি মনে রাখার কৌশল আপনাদের সাথে শেয়ার করব। যে কৌশলের মাধ্যমে আপনি খুব সহজে পর্যায় সারণি মনে রাখতে পারবেন। এই কৌশলটি আয়ত্ত করতে আপনার ১০ মিনিটের মতোন সময় লাগবে।
রসায়ন ভালোভাবে বুঝতে গেলে সকল মৌলের নাম মুখস্ত রাখা এবং সকল মৌল সম্পর্কে বিভিন্ন তথ্য যেমন মৌলের ভর, মৌলের ইলেক্ট্রন, প্রোটন ও নিউট্রন সংখ্যা, মৌলের জারণ সংখ্যা জানতে হবে। আর এই সকল তথ্য আমরা কেবল মাত্র পর্যায় সরণি থেকে পেতে পারি। পর্যায় সারণি ভালোভাবে মনে রাখলে রসায়ন অনেখানি সহজ হয়ে যাবে।
কিন্তু পর্যায় সারণি মনে রাখা অত সহজ নয়। ১১৮ টি মৌল রয়েছে বর্তমানের আধুনিক পর্যায় সারণিতে। আর এই সকল মৌলের বিভিন গ্রুপ, ব্লক, প্রতীক, পারমাণবিক সংখ্যা ইত্যাদি রয়েছে। তবে পর্যায় সারণি ভালোভাবে মনে রাখলে যেকোন মৌলের ভর, পারমাণবিক সংখ্যা, প্রতীক ইত্যাদি সকল কিছু আয়ত্তে আনা যায়। পর্যায় সারণি মনে রাখা একটুখানি কঠিন তাই অনেকে পর্যায় সারণি মনে রাখার কৌশল খুঁজে থাকে। যেহেতু আপনিও পর্যায় সারণি মনে রাখার কৌশল খুঁজছেন তাহলে এই আর্টিকেলটি থেকে কৌশলটি দেখে নিন।
নবম-দশম শ্রেণিতে থাকাকালীন আমিও এই পর্যায় সারণি মনে রাখার কৌশল অবলম্বন করে পর্যায় সারণি মনে রেখেছিলাম। যা আমার একাদশ ও দ্বাদশ শ্রেণিতেও কাজে এসেছিল। আমার খুব ভালো লাগছে আপনাদের সাথে এই পর্যায় সারণি মনে রাখার কৌশলটি শেয়ার করব বলে। যদিও অনেকেই এই কৌশল সম্পর্কে অবগত। তাহলে চলুন পর্যায় সারণি সম্পর্কে কিছু তথ্য জেনে নিয়ে পর্যায় সারণি মনে রাখার কৌশলটি দেখে নিই।
Table of Contents
পর্যায় সারণি কাকে বলে?
পর্যায় সারণি মনে রাখার কৌশল জানার চলুন আগে সংক্ষেপে জেনে নেই পর্যায় সারণি আসলে কাকে বলে। আসলে পর্যায় সারণি হচ্ছে এমন একটি সারণি যেখানে মৌলগুলোকে ক্রম অনুসারে সাজিয়ে রাখে হয়েছে। বর্তমানে আমরা যে পর্যায় সারণি দেখতে পাই সেটি পর্যায় সারণির সবচেয়ে আধুনিক রূপ। তাই একে আধুনিক পর্যায় সারণি বলা হয়।
পর্যায় সারণিতে মৌলগুলোকে স্থান দেওয়ার ক্ষেত্রে মৌলের পারমাণবিক সংখ্যা ও ইলেক্ট্রন বিন্যাসকে ভিত্তি হিসাবে ধরা হয়। আধুনিক পর্যায় সারণির সূত্র হচ্ছে – মৌলসমূহের ভৌত ও রাসায়নিক ধর্মাবলি এদের পারমাণবিক সংখ্যা বৃদ্ধির সাথে পর্যায়ক্রমে আবর্তিত হবে।
পর্যায় সারণি ছবি
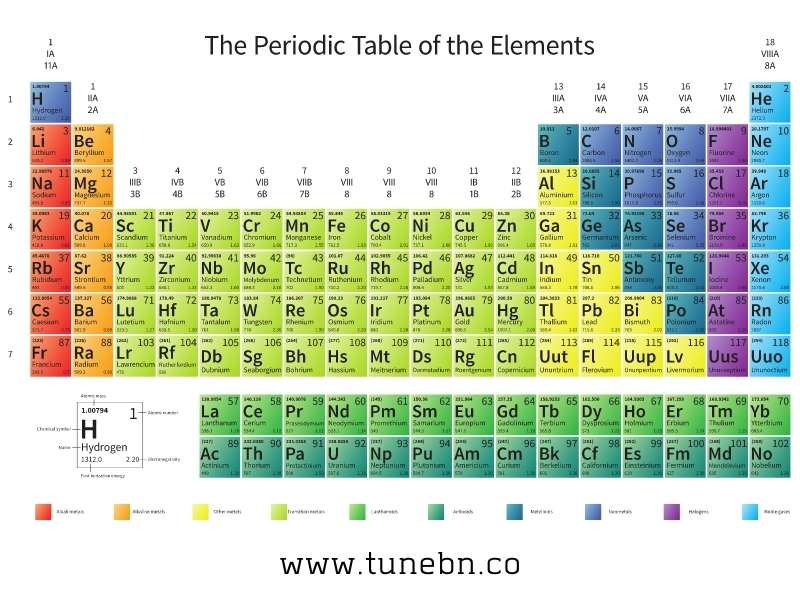
পর্যায় সারণি মনে রাখার কৌশল
পর্যায় সারণি মনে রাখার কৌশল হলো ছন্দ আকারে মুখস্ত রাখা। ছন্দ আকারে পর্যায় সারণির গ্রুপ ও পর্যায়ের সকল মৌলের নাম মুখস্ত রাখলে সহজেই পর্যায় সরণি মনে করা যাবে। অনেক ছাত্র-ছাত্রী পর্যায় সারণি মনে রাখার কৌশল হিসাবে এই উপায়টি মেনে চলে। আপনিও যদি এই কৌশল অনুসরণ করেন তাহলে ১০ মিনিটের মধ্যে পর্যায় সারণি শিখে ফেলতে পারবেন।
আপনার হয়তো জানেন যে পর্যায় সারণিতে ১৮ টি গ্রুপ ও ৭ টি সারি বা পর্যায় রয়েছে। বিভিন্ন গ্রুপের ও সারির মৌলের মধ্যে ভিন্ন ভিন্ন পার্থক্য রয়েছে। যেমনঃ গ্রুপ 1 এর মৌলগুলো ক্ষার ধর্মী, গ্রুপ 2 এর মৌলগুলো আবার মৃৎক্ষার ধাতু। গ্রুপ ও সারণির উপর ভিত্তি করে যদি আমরা পর্যায় সারণি মনে রাখার কৌশল শিখে নেই তাহলে যেকোন মৌলের নাম দেখে তা কোন গ্রুপ, কোন পর্যায়ে রয়েছে তা সহজেই বলে দিতে পারব। এর পাশপাশি মৌলটিএ বৈশিষ্ট্য কিরূপ তাও বলে পারব।
পর্যায় সারণির গ্রুপের মৌলগুলো মনে রাখার কৌশল
তাহলে প্রথমে গ্রুপ অনুযায়ী পর্যায় সারণি মনে রাখার কৌশলটি জেনে এই। Group 1A থেকে Group 8A পর্যন্ত মোট ৮ টি গ্রুপের মৌলে নাম মনে রাখার কৌশল নিম্নে দিয়ে দিলাম।
গ্রুপ 1A
গ্রুপ 1A তে মোট ৭ টি মৌল রয়েছে। এই সাতটি মৌলই ক্ষার ধর্মী অর্থাৎ এরা Alkail Metal। পানির সাথে বিক্রিয়ায় এই সকল মৌলগুলো হাইড্রোজেন গ্যাস ও ক্ষার দ্রবণ তৈরি করে।
মৌলগুলোর প্রতীকঃ H, Li, Na, K, Rb, Cs, Fr
মনে রাখার কৌশলঃ
- হে লি না কে রুবি সাজাবে ফ্রান্সে
- হা লায় না কি রাবিতে কাশ ফেলেছে
- হা লিনা কে রুবিনা ছেঁচে ফেলেছে
উদাহরণ সহ মৌলের নামঃ
- হে – H – Hydrogen (হাইড্রোজেন)
- লি – Li – Lithum (লিথিয়াম)
- না – Na – Sodium (সোডিয়াম)
- কে – K – Potassium (পটাশিয়াম)
- রুবি – Rb – Rubidium (রুবিডিয়াম)
- সাজাবে – Sc – Saesium (সিজিয়াম)
- ফ্রান্সে – Fr – Fransium – (ফ্রান্সিয়াম)
গ্রুপ 2A
গ্রুপ 2A তে মোট মৌল রয়েছে ৬ টি। আর এই সকল মৌলগুলো হচ্ছে মৃৎ ক্ষার ধাতু। এই ধাতুগুলো অনেকটাই ক্ষার ধাতুর মতোন।
মৌলগুলোর প্রতীকঃ Be, Mg, Ca, Sr, Ba, Ra
মনে রাখার কৌশলঃ
- বিধবা মায়ের ক্যাডার সন্তান বাদশাহ রহিম
- বিরিয়ানি মোগলাই কাবাব সরিয়ে বাটিতে রাখ
- বিধবা মহিলা কা সার বাসনে রাধে
উদাহরণ সহ মৌলের নামঃ
- বিধবা – Be – Beryllium (বেরিলিয়াম)
- মায়ের – Mg – Magnesium (ম্যাগনেসিয়াম)
- ক্যাডার – Ca – Calcium(ক্যালসিয়াম)
- সন্তান – Sr – Stronsium(স্ট্রানসিয়াম)
- বাদশাহ – Ba – Barium(বেরিয়াম)
- রহিম – Ra – Radium(রেডিয়াম)
গ্রুপ 3A
গ্রুপ 3A তে মোট মৌল সংখ্যা ৫ টি।
মৌলগুলোর প্রতীকঃ B, Al, Ga, In, Ti
মনে রাখার কৌশলঃ
- বরুন অল্পতেই গেল ইন্ডিয়া তে
- বাংলাদেশ আওয়ামীলীগ গেল ইন্ডিয়া ট্যুরে
- বলে এলাম জাই য়েন তাইলে
উদাহরণ সহ মৌলের নামঃ
- বরুন – B – Born (বোরন)
- অল্পতেই – Al – Aluminium (অ্যালুমিনিয়াম)
- গেল – Ga – Gallium (গ্যালিয়াম)
- ইন্ডিয়া – In – Indium (ইন্ডিয়াম)
- তে – Tl – Thallium (থেলিয়াম
গ্রুপ 4A
গ্রুপ 4A তে মৌলের সংখ্যা রয়েছে ৫ টি। এই মৌলগুলোর নাম মনে রাখার কৌশল চলুন জেনে নেই।
মৌলগুলোর প্রতীকঃ C, Si, Ge, Sn, Pb
মনে রাখার কৌশলঃ
- কলিকাতা সিটিতে গেলে সোনা পাবে
- কাদঁলে শার্ট গেন্জি স্যান্ডেল পাবে
- ছি! সিলেট গেলেন? সমস্যায় পড়বেন
উদাহরণ সহ মৌলের নামঃ
- কলিকাতা – C – Carbon (কার্বন)
- সিটিতে – Si – Silicon (সিলিকন)
- গেলে – Ge – Germanium (জামিনিয়াম)
- সোনা – Sn – Tin (টিন)
- পাবে – Pb – Lead (লেড বা সিসা)
গ্রুপ 5A
গ্রুপ 5A তে মোট মৌল রয়েছে ৫ টি। মৌলগুলোর নাম মনে রাখার কৌশল নিম্নে দেওয়া রয়েছে।
মৌলগুলোর প্রতীকঃ N, P, A,s Sb, Bi
মনে রাখার কৌশলঃ
- নাই প্রিয়া আজ সবই বিরহের
- না ফিজ আছে আন্টির বাসায়
- নাই পারুল আছে সাবিনা বিয়ান
উদাহরণ সহ মৌলের নামঃ
- নাই – N – Nitrogen (নাইট্রোজেন)
- প্রিয়া – P – Phosphorus (ফসফরাস)
- আজ – As – A arsenic (আর্সেনিক)
- সবই – Sb – Antimony (এন্টিমনি)
- বিয়ান – Bi – Bismath (বিসমাথ)
গ্রুপ 6A
গ্রুপ 6A তে মোট মৌল রয়েছে ৫ টি। গ্রুপ ৬কে চালকোজেন গ্রুপ বলা হয়ে থাকে।
মৌলগুলোর প্রতীকঃ O, S, Se, Te, Po
মনে রাখার কৌশলঃ
- অফিস শেষে সেলিনা টেলিফোন পেল
- ও এস এস-ই তে পড়ে
- ওর ছোট ছেলেটা টেবিলে পড়ে
উদাহরণ সহ মৌলের নামঃ
- অফিস – O – Oxygen (অক্সিজেন)
- শেষে – S – Sulfur (সালফার)
- সেলিনা – Se – Selenium (সেলেনিয়াম)
- টেলিফোন – Te – Tellurium (টেলুরিয়াম)
- পেল – Po – Polonium (পোলেনিয়াম)
গ্রুপ 7A
গ্রুপ 7A তে অবস্থিত মোট ৫ টি মৌলকে একত্রে হ্যালোজেন (halogen) বলে। হ্যালোজেন শব্দের অর্থ লবণ গঠনকারী (salt maker)। এরা সর্ববহিঃস্থ শক্তিস্তরে একটি ইলেকট্রন গ্রহণের মাধ্যমে হ্যালাইড আয়ন তৈরি করে। হ্যালোজেনসমূহের মূল উৎস সামুদ্রিক লবণ।
মৌলগুলোর প্রতীকঃ F, Cl, Br, I, At
মনে রাখার কৌশলঃ
- ফখরুলের ক্লোনটি বড়ই ইডি য়েট
- ফেল করলেও আইজ বাড়িতে আসতাম
- ফ্লোর কলনীর বাসায় আন্টি আছে
উদাহরণ সহ মৌলের নামঃ
- ফখরুলের – F – Florin (ফ্লোরিন)
- ক্লোনটি – Cl – Chlorine (ক্লোরিন)
- বড়ই – Br – Bromine (ব্রোমিন)
- ইডি – I – Iodine (আয়োডিন)
- য়েট – At – Astatine (অ্যাস্টেটাইন)
গ্রুপ 8A
VIIIA বা ‘O’ গ্রুপকে বলা হয় নিষ্ক্রিয় গ্যাস বা ইনার্ট গ্যাস বা noble gas, Rare gas, অভিজাত গ্যাস, বিরল গ্যাস।
মৌলগুলোর প্রতীকঃ H, Ne, Ar, Kr, Xe, Rn
মনে রাখার কৌশলঃ
- হে না আর করিম যাবে রমনায়
- হিলি নিলি আর কৃপা যাইবে রংপুর
উদাহরণ সহ মৌলের নামঃ
- হে – He – Helium (হিলিয়াম)
- না – Ne – Neon (নিয়ন)
- আর – Ar – Argon (আর্গন)
- করিম – Kr – Krypton (ক্রিপ্টন)
- যাবে – Xe – Xenon (জেনন)
- রমনায় – Rn – Radon (রাডন)
অবস্থান্তর মৌলগুলো মনে রাখার কৌশল
পর্যায় সারণিতে Group 3 থেকে Group 11 গ্রুপে অবস্থিত মৌলসমূহ অবস্থান্তর মৌল (Transition Meta) হিসেবে পরিচিত। অবস্থান্তর মৌলসমূহের নিজস্ব বর্ণ রয়েছে। এরা ধাতব পদার্থ হিসেবে প্রচুর ব্যবহৃত হয়। পর্যায় সারণি মনে রাখার কৌশলে এই মৌলগুলো কিভাবে মনে রাখবেন এখন সেই কৌশল জেনে নেই।
গ্রুপ 1B
এই গ্রুপের মৌল সমুহ কে মুদ্রা ধাতু বলা হয়। মৌলগুলো মনে রাখার কৌশল নিম্নে রয়েছে।
মৌলগুলোর প্রতীকঃ Cu, Ag, Au
মনে রাখার কৌশলঃ
- কোথায় ছিলো সোনা
উদাহরণ সহ মৌলের নামঃ
- কোথায় – Cu – Copper (কপার)
- ছিলো – Ag – Silver (সিলভার)
- সোনা – Au – Gold (গোল্ড)
গ্রুপ 2B
এই গ্রুপের ধাতু উদায়ী। মোট ৪টি মৌল এই গ্রুপে রয়েছে।
মৌলগুলোর প্রতীকঃ Zn, Cd, Hg, Cn
মনে রাখার কৌশলঃ
- জিৎও ক্যাডরিনা পেলো কলা
উদাহরণ সহ মৌলের নামঃ
- জিৎ – Zn – Zinc (জিংক)
- ক্যাডরিনা – Cd – Cadmium (ক্যাডমিয়াম)
- পেলো – Hg – Mercury (পারদ বা মার্কারি)
- কলা – Cn- Copernicium (কপারনিসিয়াম)
গ্রুপ 8B
এই গ্রুপের মৌলগুলো চৌম্বকীয় শ্রেণী ধাতু।
মৌলগুলোর প্রতীকঃ Fe, Co, Ni, Ru, Rh, Pd, Os, Ir, Pt, Hs, Mt, Ds
মনে রাখার কৌশলঃ এই গ্রুপের মৌলগুলোর নাম মনে রাখার জন্য কোন ছন্দ নেই।
উদাহরণ সহ মৌলের নামঃ
- Fe – Iron (লোহা বা আয়রন)
- Co – Cobalt (কোবাল্ট)
- Ni – Nickel (নিকেল)
- Ru – Ruthenium (রুথেনিয়াম)
- Rh – Rhodium( রোডিয়াম)
- Pd – Palladium (প্যালাডিয়াম)
- Os – Osmium (অসমিয়াম)
- Ir – Eridium (ইরিডিয়াম)
- Pt – Platinum (প্লাটিনাম)
- Hs – Hassium (হ্যাসিয়াম )
- Mt – Metnerium (মিটনেরিয়াম)
- Ds – Damstadium (ডামস্টেডিয়াম)
পর্যায় সারণির পর্যায়ের মৌলগুলো মনে রাখার কৌশল
পর্যায় সারণিতে মোট ৭টি পর্যায় রয়েছে। এই ৭টি পর্যায়ের মৌলগুলোর নাম কিভাবে মনে রাখবেন চলুন এখন তা জেনে নেই। পর্যায় সারণি মনে রাখার কৌশলে এই পর্যায় বা সারিগুলো অনেক গুরুত্বপূর্ণ।
পর্যায় ১
পর্যায় ১ এ মাত্র ২ টি মৌল রয়েছে।
মৌলগুলোর প্রতীকঃ H, He
মনে রাখার কৌশলঃ
- হ হি
উদাহরণ সহ মৌলের নামঃ
- হ – H – Hydrogen (হাইড্রোজেন)
- হি – He – Helium (হিলিয়াম)
পর্যায় ২
পর্যায় ২ এ মোট মৌল রয়েছে ৮টি। এই ৮ট্টি মৌলের নাম কিভাবে মনে রাখবেন তা এখন চলুন জেনে নেই।
মৌলগুলোর প্রতীকঃ Li, Be, B, C, N, O, F, Ne
মনে রাখার কৌশলঃ
- লি বেন? বেনী চুড়ি? নিপস্টিক ও ফা নি
উদাহরণ সহ মৌলের নামঃ
- লি – Li – Lithium (লিথিয়াম)
- বেন – Be – Beryllium (বেরেলিয়াম)
- বেনী – B – Boron (বোরন)
- চুড়ি C – Carbon (কার্বন)
- নিপস্টিক – N – Nitrogen (নাইট্রোজেন)
- ও – O – Oxygen (অকিজেন)
- ফা – F – Fluorine (ফ্লোরিন)
- নি – Ne – Neon (নিয়ন)
পর্যায় ৩
পর্যায় ৩ এর মৌলগুলোর নাম মনে রাখার কৌশল চলুন জেনে নেই। এই পর্যায়ে ৮টি মৌল রয়েছে।
মৌলগুলোর প্রতীকঃ Na, Mg, Al, Si, P, S, Cl, Ar
মনে রাখার কৌশলঃ
- না! মগা আলু ছিলতে পারে সব কিলি য়ার
উদাহরণ সহ মৌলের নামঃ
- না – Na – Sodium
- মগা – Mg – Mangnesium
- আলু – Al – Aluminium (অ্যালুমিনিয়াম)
- ছিলতে – Si – Silicon (সিলিকন)
- পারে – P – Phosphorus (ফসফরাস)
- সব – S – Sulphur (সালফার)
- কিলি – Cl – Chlorine (ক্লোরিন)
- য়ার – Ar – Argon (আর্গন)
পর্যায় ৪
পারমানবিক সংখ্যা 21-30 এর মৌলগুলো পর্যায় ৪ এ রয়েছে। এগুলো মনে রাখার কৌশল নিম্নে দিয়ে দিলাম।
মৌলগুলোর প্রতীকঃ Sc, Ti, V, Cr, Mn, Fe, Co, Ni, Cu, Zn
মনে রাখার কৌশলঃ
- শাহরুখ টাইটানিকে ভেসে কালো মনিষকে ফেলে কোয়েলকে নিয়ে কুয়াকাটা যাবে
- স্কুল টি ভাঙায় চেয়ার ম্যান ফের কমিশন নিয়ে কাজে যাচ্ছেন
উদাহরণ সহ মৌলের নামঃ
- শাহরুখ – Sc – Scandium (স্ক্যানডিয়াম)
- টাইটানিকে Ti – Titanium ( টিটেনিয়াম)
- ভেসে V – Vanadium (ভ্যানাডিয়াম)
- কালো – Cr – Chromium (ক্রোমিয়াম)
- মনিষকে – Mn – Manganese (ম্যাঙ্গানিজ)
- ফেলে – Fe – Iron (লোহা বা আয়রন)
- কোয়েলকে – Co – Cobalt (কোবাল্ট)
- নিয়ে – Ni – Nickel (নিকেল)
- কুয়াকাটা – Cu – Copper (কপার)
- যাবে – Zn – Zinc (জিংক)
পর্যায় ৫
পারমানবিক সংখ্যা 39 থেকে 48 এর মৌলসমূহ এই পর্যায়ে অবস্থান করে। পর্যায় ৫ এ মোট মৌল রয়েছে ১০টি।
মৌলগুলোর প্রতীকঃ Y, Zr, Nb, Mo, Tc, Ru, Rh, Pd, Ag, Cd
মনে রাখার কৌশলঃ
- ইতি ও জেরিন নাইরোবিতে মোবাইল সহ রুথের রোড টি দিয়ে পালাবার আগে কাঁদছিল
- ইওর জ্বর নামবে মন টাকে আরো রেস্ট-হতে দাও পারলে আগে কাঁদো
উদাহরণ সহ মৌলের নামঃ
- ইতি – Y – Yttrium (ইট্রিয়াম)
- জেরিন – Zr – Zirconium (জিরকোনিয়াম
- নাইরোবিতে – Nb – Niobium (নিওবিয়াম)
- মোবাইল – Mo – Molybdenum (মলিবডেনাম)
- টি – Tc – Technitium (টেকনেসিয়াম)
- রুথের – Ru – Ruthenium (রুথেনিয়াম)
- রোড – Rh – Rhodium (রোডিয়াম)
- পালাবার – Pd – Palladium (প্যালাডিয়াম)
- আগে – Ag – Silver (সিলভার)
- কাঁদছিল – Cd – Cadmium (ক্যাডমিয়াম)
পর্যায় ৬
পর্যায় ৬ এর মৌলগুলোর পারমাণবিক সংখ্যা ৫৭ থেকে ৮০ এর মধ্যে।
মৌলগুলোর প্রতীকঃ La, Hf, Ta, W, Re, Os, Ir, Pt, Au, AG, Hg
মনে রাখার কৌশলঃ
- লাকি ও হানিফ টাইটানিকে করে ওয়াবিকে রেখে আবার ইউরোপে প্লাটিনাম ও গোল্ড পায়
উদাহরণ সহ মৌলের নামঃ
- লাকি – La – Lanthanum (ল্যানথানাইড সিরিজ)
- হানিফ – Hf – Hafnium (হাফনিয়াম)
- টাইটানিকে – Ta – Tantalum (ট্যান্টালুম)
- ওয়াবিকে – W – Tungsten (টাংস্টেন)
- রেখে – Re – Rhenium (রেনিয়াম)
- আবার – Os – Osmium (অসমিয়াম)
- ইউরোপে – Ir – Eridium (ইরিডিয়াম)
- প্লাটিনাম – Pt – Platinum (প্লাটিনাম)
- গোল্ড – Au – Gold (গোল্ড)
- পায় – Hg – Mercury (পারদ বা মাকারি)
পর্যায় ৭
পারমানবিক সংখ্যা 89 থেকে 112 এর মৌলগুলো পর্যায় ৭ এ অবস্থান করে।
মৌলগুলোর প্রতীকঃ Ac, Rf, Db, Sg, Bh, Hs, Mt, Ds, Rg, Cn
মনে রাখার কৌশলঃ
- আখির ছেলে রাফি ডুবাই সাগরে বাহিরে ভেসে হাফেজ আর মতিকে দেশে রেগে চিনেছে
উদাহরণ সহ মৌলের নামঃ
- আখির – Ac – Actinium (অ্যাকটিনাইড সিরিজ )
- রাফি – Rf – Rutherfordium (রাদারফোর্ডিয়াম)
- ডুবাই – Db – Dubnium (ডুবনিয়াম)
- সাগরের – Sg – Seoborgium( সিওবোগিয়াম)
- বাহিরে -Bh – Bohrium (বোহরিয়াম)
- হাফেজ – Hs – Hassium (হ্যাসিয়াম )
- মতিকে – Mt – Metnerium (মিটনেরিয়াম)
- দেশে – Ds – Damstadium (ডামস্টেডিয়াম)
- রেগে – Rg – Roentgenium (রন্টজেনিয়াম)
- চিনেছে – Cn – Copemicium (কপারনিসিয়াম)
ল্যান্থানাইড ও অ্যাক্টিনাইড সিরিজের মৌলগুলো মনে রাখার কৌশল
ল্যান্থানাইড ও অ্যাক্টিনাইড সিরিজের মৌলগুলো যথাক্রমে পর্যায় সারণির পর্যায় ৬ ও পর্যায় সারণির পর্যায় ৭ এর মধ্যে অন্তভুক্ত। পর্যায় সারণি মনে রাখার কৌশলে এই মৌলগুলো কিভাবে মনে রাখবেন চলুন তা জেনে নেই।
ল্যান্থানাইড
মৌলগুলোর প্রতীকঃ Ce, Pr, Nd, Pm, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tm, Yb, Lu
মনে রাখার কৌশলঃ ছেলের প্রীতি এন্ড প্রেম সমান ইউরোপ গুড তবে ডাইরিয়া হয় এর টমেটো ইয়লো ব্লু
অ্যাক্টিনাইড
মৌলগুলোর প্রতীকঃ Th, Pa, U, Np, Pu, Am, Cm, Bk, Cf, Es, Fm, Md, No, Lr
মনে রাখার কৌশলঃ থাকলে পাশে ইউ এনপি পুঁথি আমার কমেনা বিকেলে ক্যাফেতে এসে এফ এম মোডে নুডলস লাড়ি
পর্যায় সারণি মনে রাখার কৌশল শেয়ার করে দিলা আপনাদের সাথে। অনেকেই এই কৌশল অবলম্বন করে পর্যায় সারণি মনে রাখে।
প্রায়শই জিজ্ঞাসিত প্রশ্নাবলী
পর্যায় সারণি মনে রাখার কৌশল নিয়ে লেখা এই আর্টিকেলটি সম্পর্কিত কিছু প্রশ্ন ও প্রশ্নের উত্তর চলুন জেনে নেই।
পর্যায় সারণি মনে রাখার কৌশল কি?
পর্যায় সারণি মনে রাখার কৌশল এমন একটি কৌশল যে কৌশল অবলম্বন করে পর্যায় সারণির সকল মৌলের নাম, মৌলের বৈশিষ্ট্য ইত্যাদি তথ্য মনে রাখা যবে।
পর্যায় সারণি কি মনে রাখা কঠিন?
সম্পূর্ণ পর্যায় সারণি মনে রাখা একটু হলেও কঠিন। তবে এই আর্টিকেলে দেখা কৌশল অবলম্বন করে সহজে পর্যায় সারণি মনে রাখে যাবে।
পর্যায় সারণি কেন প্রয়োজন?
সহজেই যেকোন মৌলের অবস্থান, গঠন, ধর্ম, পারমাণবিক সংখ্যা জানার জন্য পর্যায় সারণি প্রয়োজন।
শেষ কথা
এই ছিল পর্যায় সারণি মনে রাখার কৌশল নিয়ে আমাদের এই আর্টিকেল। আমি আশা করছি আর্টিকেলে দেখানো পর্যায় সারণি মনে রাখার কৌশল অবলম্বন করে আপনি পর্যায় সারণি মনে রাখতে পারবে। বেশীরভাগ ছাত্র-ছাত্রী সাধারণত এই কৌশল অবলম্বন করে পর্যায় সারণি মনে রাখে। আপনিও যদি সহজে মনে রাখতে চান তবে কৌশলটি অবলম্বন করুন। প্রতটি ছন্দ ভালোভাবে মুখস্ত রাখুন তাহলে আপনার কাছে বিষয়টি অরো অনেক সহজ হবে।
ধন্যবাদ আপনাকে টিউনবিএনে ভিজিট করে আমাদের সাথে থেকে আর্টিকেলটি পড়ার জন্য। এই ধরনের আরো অনেক আর্টিকেল পেতে নিয়মিত ভিজিট করুন আমাদের ওয়েবসাইটে। আর্টিকেলটি নিয়ে আপনার যেকোন মতামত বা প্রশ্ন করতে কমেন্ট করুন।






অনেক অনেক বেশি thanks🥰🥰🥰❤️❤️❤️❤️❤️👍👍👍👍😇😇😇😇😇